acido 3′-ammino-2′-idrossi-[1,1'-bifeni]-3-carbossilico
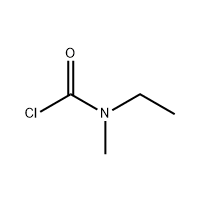
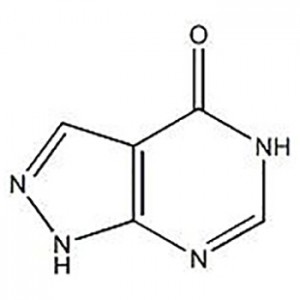
acido 3′-ammino-2′-idrossi-[1,1'-bifeni]-3-carbossilico
L'acidu 3'-Amino-2'-hydroxy-[1,1'-bipheny]-3-carboxylic hè usatu cum'è l'intermediu di Eltrombopag.
Eltrombopag, sviluppatu da GlaxoSmithKline (GSK) in u Regnu Unitu è più tardu sviluppatu in cunghjunzione cù Novartis in Svizzera, hè u primu è l'unicu agonista di u receptore TPO non peptidico appruvatu in u mondu.Eltrombopag hè statu appruvatu da a US FDA in 2008 per u trattamentu di purpura trombocitopenica idiopatica (ITP), è in 2014 per u trattamentu di l'anemia aplastica severa (AA).Hè ancu a prima droga appruvata da a FDA US per u trattamentu di l'AA in l'ultimi 30 anni.
In dicembre 2012, a FDA di i Stati Uniti hà appruvatu Eltrombopag per u trattamentu di trombocitopenia in i malati cù l'hepatitis C crònica (CHC), in modu chì i malati di l'hepatitis C cun prognosi poveru per via di un conte di piastrinu bassu pò inizià è mantene a terapia standard basata in interferone per e malatie di u fegatu.U 3 di ferraghju di u 2014, GlaxoSmithKline hà annunziatu chì a FDA hà cuncessu a qualificazione di droga di trattamentu avanzata di Eltrombopag per u trattamentu di l'hemopenia in i malati cù l'anemia aplastica (SAA) chì ùn anu micca rispostu cumplettamente à l'immunoterapia.U 24 d'aostu di u 2015, a FDA di i Stati Uniti hà appruvatu Eltrombopag per u trattamentu di trombocitopenia in adulti è zitelli di 1 annu è più cù trombocitopenia immune crònica (ITP) chì anu una risposta insufficiente à corticosteroidi, immunoglobuline o splenectomia.U 4 di ghjennaghju di u 2018, Eltrombopag hè statu appruvatu per esse listatu in Cina per u trattamentu di a trombocitopenia immune primaria (ITP).


![Acidu 3′-ammino-2′-idrossi-[1,1'-bifeni]-3-carboxylic Image Featured Image](http://cdn.globalso.com/jindunchem-med/image351.png)
![acido 3′-ammino-2′-idrossi-[1,1'-bifeni]-3-carbossilico](http://cdn.globalso.com/jindunchem-med/image351-300x300.png)
![6-tetra-O-acteil-1-C-[4-cloro-3-[[4-[[(3S)-tetraidrofu-ran-3-il]ossi]fenile]](http://cdn.globalso.com/jindunchem-med/0ecf55f0-300x300.jpg)